Nell’articolo “Proteine: cosa sono e dove si trovano” abbiamo descritto quante funzioni diverse possono svolgere: enzimi che accelerano reazioni vitali, anticorpi che ci proteggono, ormoni che regolano l’organismo, proteine strutturali che compongono i tessuti…
Eppure, ciò che permette a una proteina di riconoscere un bersaglio, catalizzare una reazione, trasportare una molecola o dare resistenza a un tessuto è sempre la sua struttura tridimensionale.
Relazione tra struttura e funzione delle proteine
Quando parliamo di proteine, la prima cosa da ricordare è che non esiste funzione senza una forma precisa. Immagina la proteina come una chiave: funziona solo se mantiene esattamente la sua forma. Se la chiave si deforma, non apre più nessuna porta. Allo stesso modo, una minima variazione nella struttura può rendere una proteina inattiva o inefficace.
Ecco perché l’organismo investe tanta energia nel ripiegamento corretto, nel “controllo qualità” delle proteine e nel loro mantenimento. La forma è il loro linguaggio, e la funzione delle proteine dipende interamente da quel linguaggio. Ma andiamo a vedere nel dettaglio come è strutturata una proteina!
Amminoacidi: i mattoncini che formano le proteine
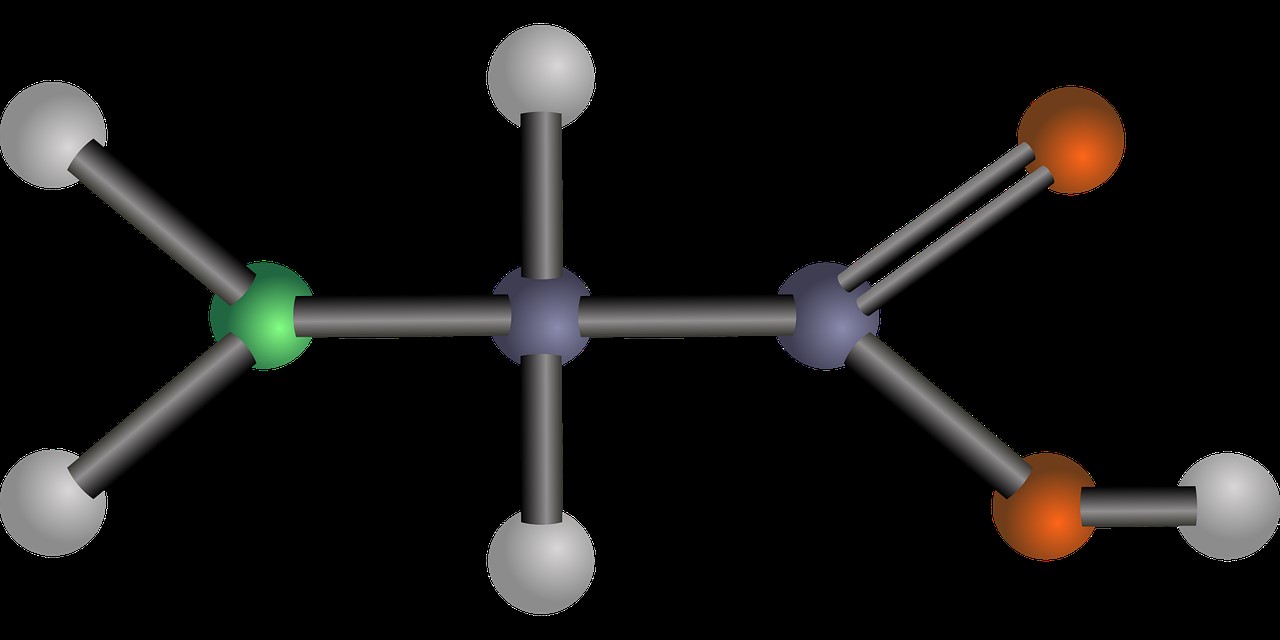
Alla base di ogni proteina troviamo gli amminoacidi, piccoli composti organici formati da un atomo centrale di carbonio (carbonio α) che si lega con:
- un gruppo amminico (–NH₂),
- un gruppo carbossilico (–COOH),
- un atomo di idrogeno,
- una catena laterale che in chimica viene indicata con la lettera R, ed è diversa per ciascun amminoacido.
Una proteina è una molecola formata da tanti amminoacidi diversi. Nel nostro organismo ne esistono 20, alcuni dei quali sono definiti essenziali: significa che devono arrivare dall’alimentazione perché il corpo non è in grado di sintetizzarli da solo.
Per formare la proteina, gli amminoacidi si uniscono tra loro tramite dei particolari legami (definiti in chimica legami peptidici), formando lunghe catene. Gli amminoacidi hanno delle caratteristiche diverse a livello della catena laterale R: alcune di queste possono essere idrofile, capaci cioè di legarsi con l’acqua; altre al contrario sono idrofobe; alcune presentano anche delle cariche positive o negative.
È come costruire una collana: tante perle si uniscono insieme… ma la vera magia avviene quando il filo prende forma e si avvolge nello spazio! Infatti, a seconda degli amminoacidi che compongono la “collana” (e quindi delle loro caratteristiche) ci saranno delle interazioni diverse tra loro e con l’ambiente circostante, ed è questo che andrà a determinare il modo in cui avvolgersi, e dunque la struttura tridimensionale della proteina.
Strutture delle proteine
Possiamo definire quattro tipologie di strutture, una è alla base dell’altra. Vediamo quali sono:
Struttura primaria
È la semplice sequenza lineare di amminoacidi.
La sua importanza è enorme: cambiare un solo amminoacido può modificare completamente la struttura tridimensionale e la funzione della proteina. Un esempio è l’emoglobina nell’anemia falciforme; qui una sola sostituzione causa un cambiamento strutturale e funzionale significativo.
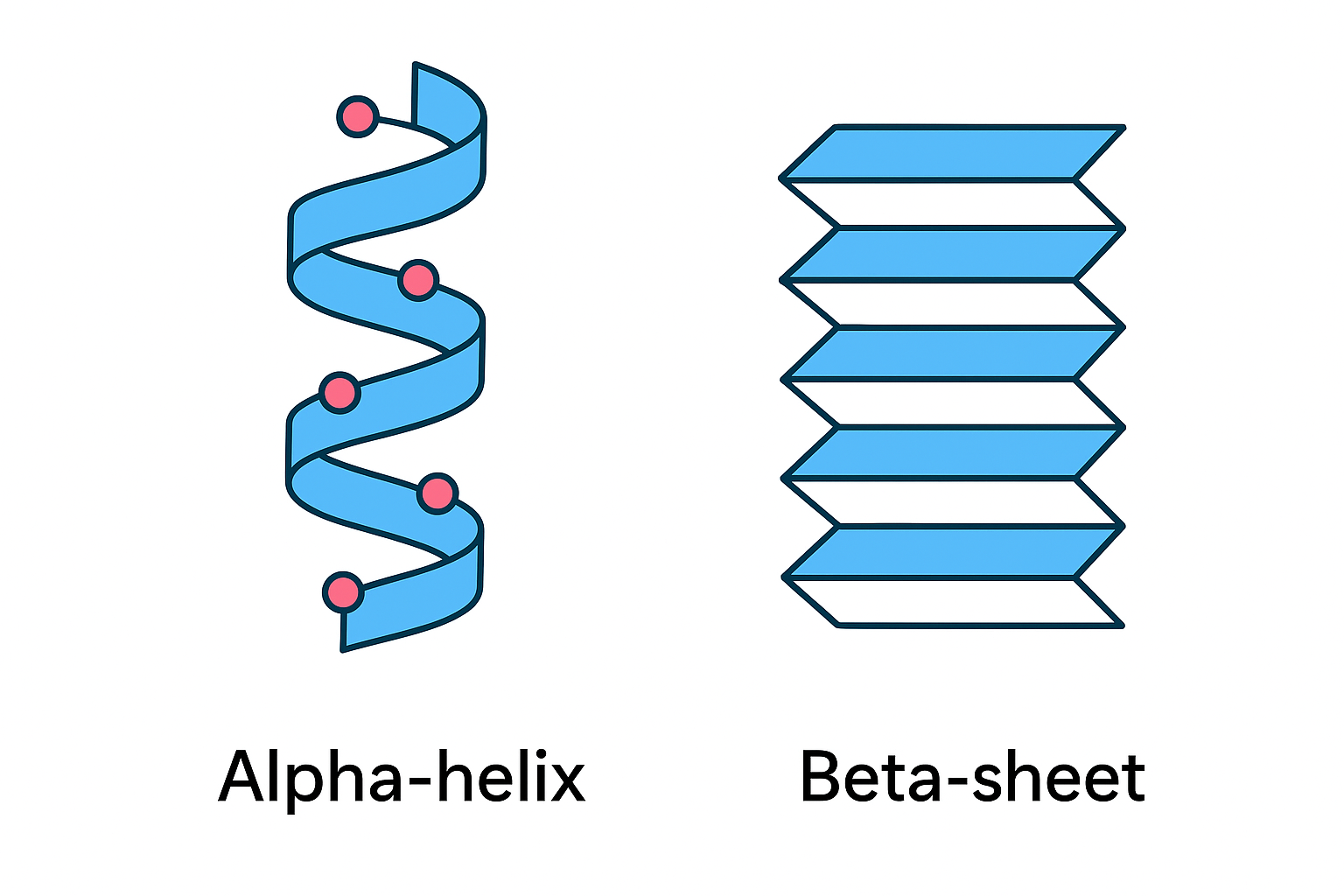
Struttura secondaria
Qui la catena inizia a ripiegarsi localmente, e vi sono due tipi di ripiegamento possibile:
- α-eliche (spirali regolari)
- β-foglietti (strutture più distese)
Questi ripiegamenti sono mantenuti dai cosiddetti legami a idrogeno.
È un po’ come quando inizi a piegare un foglio di carta per creare un origami: le prime pieghe non rappresentano ancora la forma finale, ma sono fondamentali perché guideranno tutti i passaggi successivi. Allo stesso modo, le strutture secondarie creano le prime “pieghe” che permetteranno alla proteina di ripiegarsi correttamente fino alla sua forma definitiva.
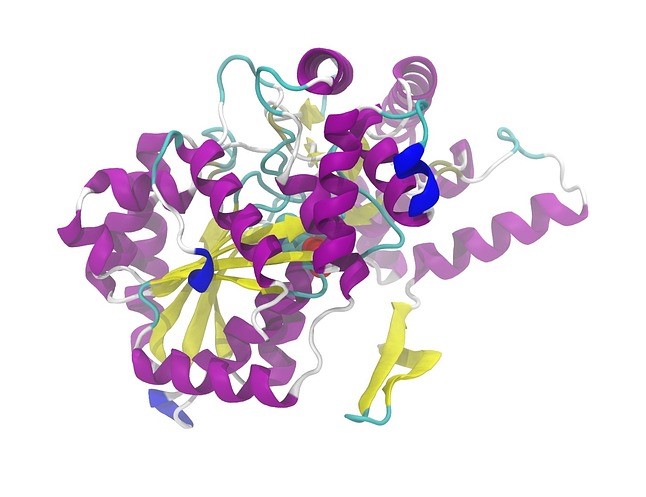
Struttura terziaria
È la forma tridimensionale completa della proteina: la catena si ripiega su se stessa fino a raggiungere la configurazione più stabile. Qui intervengono diversi tipi di legami:
• ponti disolfuro (S–S),
• interazioni idrofobiche,
• interazioni ioniche,
• legami a idrogeno.
La struttura terziaria è ciò che permette alla proteina di riconoscere molecole, legarsi a un recettore, catalizzare reazioni… insomma di esercitare la funzione per cui è stata prodotta dal nostro corpo.
Struttura quaternaria
Non tutte le proteine la possiedono. È il livello in cui più catene proteiche si uniscono per formare un complesso funzionale, come avviene ad esempio nell’emoglobina. Ogni catena contribuisce alla funzione complessiva, come strumenti in un’unica orchestra.
Alterazione della struttura proteica
Le proteine sono sensibili all’ambiente che le circonda. Cambiamenti di temperatura, pH o forza ionica possono modificarne la forma. In questi casi si tratta solitamente di modifiche temporanee, quindi ripristinando le condizioni iniziali, la struttura torna come era prima.
Un esempio che tutti conosciamo è quello della piastra per lisciare i capelli. I capelli sono costituiti soprattutto da proteine, la principale è la cheratina.
Il calore della piastra rompe temporaneamente alcuni legami a idrogeno nelle proteine del capello, permettendo alla fibra di cambiare forma. Quando c’è umidità i capelli iniziano a tornare ricci perché l’acqua presente nell’ambiente umido circostante induce la formazione di nuovi legami a idrogeno e le proteine del capello riprendono la loro forma “naturale”.
La situazione appena descritta è un esempio di denaturazione reversibile.
Alcune modifiche, invece, non sono reversibili. È il caso, ad esempio, della digestione enzimatica: gli enzimi digestivi (come la pepsina e la tripsina) spezzano i legami peptidici, riducendo la proteina a singoli aminoacidi. In questo caso la struttura primaria viene distrutta, rendendo impossibile ricostruire la proteina originale.
È una denaturazione irreversibile, fondamentale per poter assorbire gli amminoacidi e utilizzarli nel metabolismo.
Conclusione
La struttura delle proteine non è un dettaglio tecnico, ma la base per poter funzionare. Ogni interazione contribuisce a creare una forma unica, capace di svolgere compiti fondamentali per il nostro organismo. Anche le alterazioni che subiscono ci ricordano quanto esse siano dinamiche e sensibili all’ambiente.
Se siete arrivati fin qui, da oggi vedrete le proteine non solo come nutrienti, ma come ingegnose architetture biologiche, tanto dinamiche quanto utili per la nostra vita.
Riferimenti e approfondimenti:
- Alberts, B., Johnson, A., Lewis, J., Raff, M., Roberts, K., & Walter, P. (2015). Biologia molecolare della cellula (6ª ed.). Zanichelli.
- Nelson, D. L., & Cox, M. M. (2017). I principi di biochimica di Lehninger (7ª ed.). Zanichelli.
- Fliegel, L. (2023). Structure and Function of Membrane Proteins. International Journal of Molecular Sciences, 24(9), 8350.
- Chiesa, G., Kiriakov, S., & Khalil, A. S. (2020). Protein assembly systems in natural and synthetic biology. BMC Biology, 18, 35.